Neue Metabolische Strategien zur Protektion hochenergetischer Gewebe
Übersichtsarbeit - Review
Metabolische Reprogrammierung hochenergetischer Gewebe: Sertaconazol und Talarozol als innovative Strategien jenseits der Komplement-Inhibition – Ein interdisziplinäres Review zur „erworbenen Mitochondriopathie“
Autor: Cord Uebermuth - Facharzt für Augenheilkunde
Korrespondenz: @augenarzt auf steemit
Schlagwörter: Geographische Atrophie, Drug Repurposing, Sertaconazol, Talarozol, Metformin, Mitochondriopathie, Laktat-Clearance, Pankreaskarzinom, Neuropathie
Von der AMD-Prävention bis zur onkologischen Supportivtherapie: Das Potenzial von Metformin, Sertaconazol und Talarozol im Rahmen des Drug Repurposing
Grundlage
Degenerative Erkrankungen wie die geographische Atrophie (GA), der sensorineurale Hörverlust (SNHL) und die Chemotherapie-induzierte periphere Neuropathie (CIPN) teilen eine pathophysiologische Endstrecke: die mitochondriale Dysfunktion („erworbene Mitochondriopathie“). Dieser Review evaluiert das Potenzial metabolischer Modulatoren zur Resilienzsteigerung des retinalen Pigmentepithels (RPE), der cochleären Haarzellen und peripherer Nervenfasern. Basierend auf klinischen Langzeitbeobachtungen und KI-gestützten Analysen werden Metformin sowie die neuen Kandidaten Sertaconazol und Talarozol diskutiert. Es wird betont, dass die Datenlage zu Sertaconazol und Talarozol aktuell hypothetisch ist und einer dringenden klinischen Evaluation bedarf.
EINLEITUNG
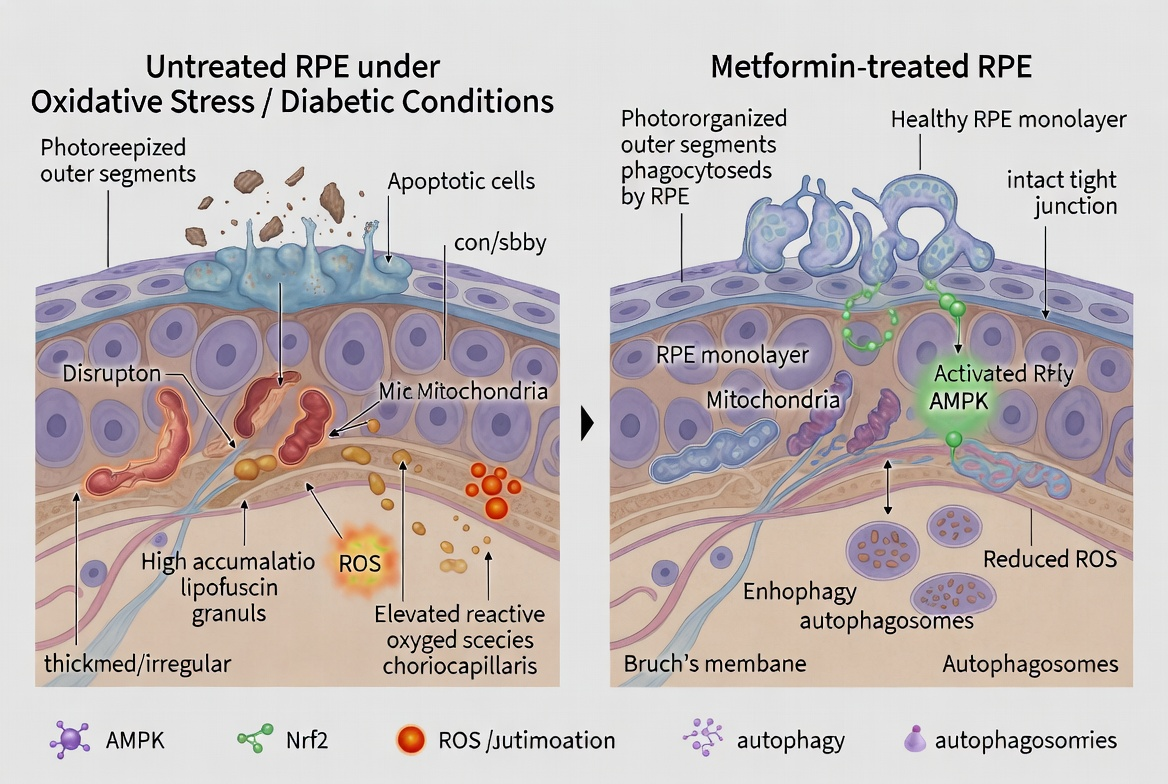
Hochenergetische Gewebe (Retina, Cochlea, Myelinscheiden) reagieren empfindlich auf Störungen der mitochondrialen Homöostase. Die GA der Makula wird zunehmend als energetisches Versagen des RPE verstanden, wobei die „metabolische Koppelung“ (Laktat-Clearance) zwischen Photorezeptoren und RPE kollabiert. Ein ähnlicher Mechanismus findet sich beim SNHL und der CIPN (insbesondere unter Platin-Therapie wie beim Pankreaskarzinom/PDAC).
KEY MESSAGES
Pathophysiologische Konvergenz: Die geographische Atrophie (GA), der sensorineurale Hörverlust (SNHL) und die platininduzierte Neuropathie (CIPN) basieren auf einer mitochondrialen Dysfunktion („erworbenen Mitochondriopathie“), charakterisiert durch energetische Erschöpfung und Laktat-Akkumulation.
Präventive Evidenz (Metformin): Langzeitdaten belegen signifikante Risikoreduktionen für AMD (-46 %), Pankreaskarzinome (-62 %) und schwere Neuropathien (-65 %).
Kritisches Zeitfenster: Das klinische Scheitern von Metformin bei manifester geographischer Atrophie (GA) der Macula in der METforMIN Studie ((p = 0,39)) verdeutlicht, dass metabolische Interventionen vor dem irreversiblen strukturellen Kollaps initiiert werden müssen.
Innovation durch Drug Repurposing: Sertaconazol und Talarozol (HHU Düsseldorf, 2026) bieten neue Ansätze zur direkten Steigerung der mitochondrialen Resilienz und Stabilisierung der Laktat-Clearance.
Hypothetischer Status: Die klinische Validierung am Menschen mittels funktioneller Diagnostik (10-2 GF, mfERG) steht noch aus und ist Gegenstand aktueller Forschung.
1. ABSTRACT
Degenerative Prozesse hochenergetischer Gewebe teilen eine gemeinsame Endstrecke: den mitochondrialen Kollaps. Dieser Review evaluiert das Potenzial metabolischer Modulatoren zur Resilienzsteigerung des retinalen Pigmentepithels (RPE), der cochleären Haarzellen und peripherer Nervenfasern. Basierend auf klinischen Langzeitbeobachtungen (Metformin-Effekt) und KI-gestützten Analysen werden Sertaconazol und Talarozol als Kandidaten zur Wiederherstellung der metabolischen Homöostase diskutiert.
2. EINLEITUNG
Hochenergetische Gewebe wie die Retina und die Cochlea sind auf eine präzise „metabolische Koppelung“ angewiesen. In der Makula fungiert das RPE als Laktat-Pumpe. Versagt diese (Mitochondriopathie), führt die resultierende lokale Azidose zur Apoptose. Ähnliche Mechanismen treiben den Hörverlust und Chemotherapie-assoziierte Nervenschäden (z. B. beim Pankreaskarzinom/PDAC) voran.
3. METABOLISCHE PROTEKTION:
DATENLAGE UND HYPOTHESEN
3.1 Geographische Atrophie und AMD
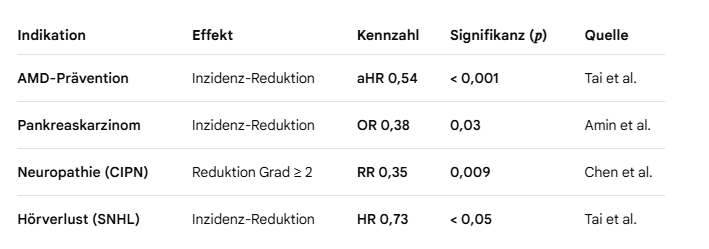
Epidemiologische Studien zeigen unter Metformin eine signifikante Risikoreduktion für AMD (aHR 0,54; p < 0,001). Die METforMIN-Studie zeigt jedoch, dass die Wirkung bei bereits manifester GA gering ist (Δ -0,03 mm/J.; p = 0,39).
Hier setzen Sertaconazol (mitochondriale Stabilisierung) und Talarozol (CYP26-Inhibition/Retinsäure-Modulation) an, um die metabolische Resilienz direkt im gefährdeten Gewebe zu erhöhen.
3.2 Onkologie: PDAC und Neuropathie-Prävention
Beim duktalen Pankreasadenokarzinom (PDAC) senkt Metformin das Inzidenzrisiko (OR 0,38). Von besonderer klinischer Relevanz ist der Schutz vor Platin-induzierten Neuropathien (CIPN), wobei Metformin das Risiko schwerer Nervenschäden um 65 % reduziert (p = 0,009).
4. STATISTISCHE ÜBERSICHT (TABELLE 1)
DISKUSSION
Die klinische Erfahrung aus drei Jahrzehnten eigener Tätigkeit deutet darauf hin, dass die rein symptomatische Therapie der trockenen Form der AMD die als geograhische Atrophie klinisch sich im Endstadium manifestiert unzureichend bleibt.
Oder anders formuliert:
Der Einsatz von metabolischen Modulatoren erfordert jedoch ein Umdenken in der Diagnostik (verstärkter Einsatz von 10-2 GF und FAF). Während Metformin primär präventiv wirkt, bieten Sertaconazol und Talarozol theoretisch das Potenzial, auch bei bereits gestressten Zellen protektiv einzugreifen. Hierzu sind weitere klinische Forschungsarbeit erforderlich um den schweren Spätformen der mitochondrialen Schädigungen der betreffenden Organstrukturen rechtzeitig entgegen zu wirken.
Take Home Message
Caveat: Die hier vorgestellten Zusammenhänge bezüglich Sertaconazol und Talarozol basieren auf klinischen Analogieschlüssen und präklinischen Daten. Die klinische Evidenz am Menschen muss in künftigen Studien (Phase I/II) erbracht werden.
6. LITERATURVERZEICHNIS
1. HHU Düsseldorf (2026): KI-Suche nach Leigh-Syndrom-Therapien.
2. Brown, E. E. et al. (2023): METforMIN Trial (Ophthalmology Science).
3. Tai, S. Y. et al. (2020): Metformin & AMD (BMC Ophthalmology).
4. Amin, S. et al. (2024): Metformin & PDAC (MDPI Cancers).
5. Chen, Q. et al. (2021): Metformin & CIPN (J. Neuroinflammation).
6. Zhu, J. et al. (2022): Metformin in SNHL (Frontiers)